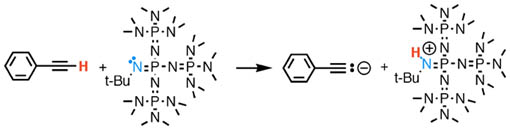

丂丂丂桳婡壔妛斀墳偵偍偄偰偼丄斀墳惈偵晉傫偩妶惈庬 (斀墳拞娫懱丗斀墳偺僪儔僀價儞僌僼僅乕僗) 傪梡偄偰丄庬乆偺曄姺斀墳傪峴偆丅廬偭偰丄桳婡壔妛斀墳傪岠棪傛偔峴傢偣傞偨傔偵偼丄偦偺斀墳拞娫懱偺惈幙傪抦傞偙偲偑昁梫偱偁傞丅庬乆偺斀墳拞娫懱偺拞偱傕丄扽慺傾僯僆儞庬偼昿斏偵梡偄傜傟傞偵傕娭傢傜偢丄偦偺夝愅偑懠偺斀墳拞娫懱偲斾傋偰抶傟偰偄傞丅偦偙偱旕嬥懏惈偺挻嫮墫婎偱偁傞僼僅僗僼傽僛儞墫婎偑庬乆偺斀墳婎幙傪扙僾儘僩儞壔偡傞惈幙傪棙梡偟偰丄扽慺傾僯僆儞庬 (斀墳拞娫懱) 偺敪惗傪帋傒偨 (忋恾嶲徠)丅僼僅僗僼傽僛儞墫婎偵傛偭偰敪惗偟偨傾僯僆儞庬偼懳僇僠僆儞偱偁傞僼僅僗僼傽僛僯僂儉僇僠僆儞偲偺娫偵嫟桳寢崌惈偑側偄偲峫偊傜傟傞丅偙偺傛偆側傾僯僆儞庬偼桳婡嬥懏帋栻 (扽慺傾僯僆儞摍壙懱埥偄偼扽慺傾僯僆儞尮) 偲斾妑偟偰丄傛傝恀偺斀墳拞娫懱 (偙偺応崌丄僇儖僶僯僆儞) 偵嬤偄忬懺偲峫偊傜傟丄傾僯僆儞庬偺夝愅偵揔偟偰偄傞偲峫偊傜傟傞丅
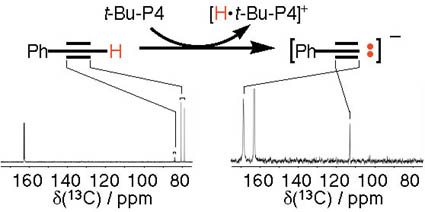
丂丂丂傑偨嬥懏僼儕乕偺僇儖僶僯僆儞偺偆偪丄娤應偝傟偨偙偲偑偁傞傕偺偼丄僄僲儔乕僩丄僗儖僼僅僯儗乕僩丄僼儖僆儗僯儖傾僯僆儞丄僼僢壔扽慺壔崌暔偵尷傜傟傞丅偙傟傜偼偄偢傟傕sp3拞怱偺扽慺偐傜扙僾儘僩儞偡傞偙偲偵傛偭偰摼傜傟傞傾僯僆儞庬埥偄偼偦偺摍壙懱偱偁傞丅偦偙偱丄Ph-C≡C-H偺僄僠僯儖僾儘僩儞傪堷偒敳偄偰摼傜傟偨丄sp扽慺忋偵 (宍幃) 揹壸傪桳偡傞傾僯僆儞庬偺NMR暘岝朄偵傛傞峔憿夝愅傪帋傒偨(娭楢榑暥)丅偦偺寢壥丄傾僙僠儕僪傾僯僆儞偺惗惉偵敽偄傾僯僆儞拞怱偺傾僙僠儗儞枛抂扽慺妀偺壔妛僔僼僩抣偑栺90 ppm傕掅帴応僔僼僩偡傞偙偲偑敾偭偨乮壓恾嶲徠乯丅偙偺掅帴応僔僼僩傪婲偙偟偨壔妛僔僼僩抣偑懨摉偱偁傞偐偳偆偐傪昡壙偡傞偨傔偵DFT寁嶼 (B3LYP/6-311++G(2d,p)) 傪峴偭偨丅DFT寁嶼偺寢壥丄傾僯僆儞拞怱偺傾僙僠儗儞枛抂扽慺妀偺壔妛僔僼僩抣偺棟榑抣偼179.6 ppm偲寁嶼偝傟丄傾僯僆儞壔偵敽偭偰傾僙僠儗儞枛抂扽慺妀偺壔妛僔僼僩抣偼掅帴応僔僼僩偡傞偙偲偑棟榑揑偵傕棤晅偗傜傟偨丅
[塸岅僞僀僩儖] Yoshinori Kondo, Masahiro Ueno and Yoshiyuki Tanaka, Organic synthesis using organic superbase, Journal of Synthetic Organic Chemistry Japan, 63, (5) 453-463 (2005).