【発表のポイント】
- 指定難病である先天性腎性尿崩症(cNDI)(注1)に対する候補薬である2型バソプレシン受容体(V2R)(注2)作動薬OPC51803とその類縁化合物(総称して、OPC5アナログ)(注3)のシグナル伝達機能を評価しました。
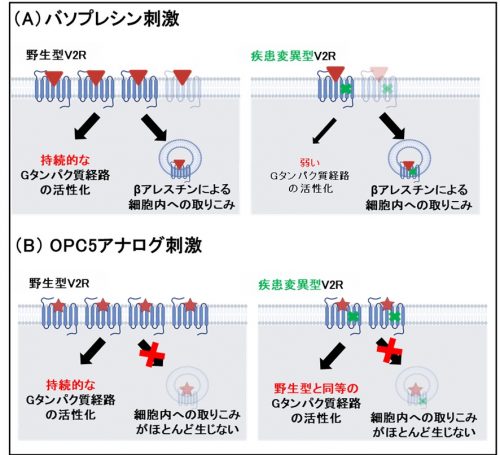
- シグナル伝達活性が低下する疾患変異型V2Rに対し、OPC5アナログは未変異型V2Rと同等のシグナル伝達を誘導することを明らかにしました。
- ドッキングシミュレーション(注4)から、OPC5アナログとバソプレシン(注5)のシグナル伝達の差異に関わる構造基盤を推定しました。
- これらの研究成果は、V2R疾患変異に応じた治療薬の開発の重要性を示しており、今後のcNDIの治療薬開発に貢献すると期待されます。
【概要】
2型バソプレシン受容体(V2R)はGタンパク質共役型受容体(GPCR)(注6)の一種であり、抗利尿ホルモンのバソプレシンと結合して細胞内のシグナルを伝達します。V2Rの機能低下型遺伝子変異は先天性腎性尿崩症(cNDI)の原因となります。現在、cNDIに対する有効な治療法の選択肢は限られています。
東北大学大学院薬学研究科の倉本律輝大学院生、木瀬亮次特任助教、井上飛鳥教授らのグループは、cNDIを引き起こす疾患変異型V2Rに対して複数のOPC5アナログの有効性を細胞アッセイ及びOPC5アナログのドッキングシミュレーションによって評価しました。その結果、OPC5アナログは細胞膜の発現量が低い疾患変異型V2Rにおいて健常人型(野生型)(注7)V2Rと同程度までGタンパク質シグナルが回復することを明らかにしました。また、OPC5アナログに特有のV2Rとの相互作用が、このシグナル伝達の差異を生み出していることが推測されました。
本研究で行った変異の種類に応じた治療戦略の選択は今後の創薬展開に貢献することが期待されます。
本研究成果は、2024年5月15日付けで科学誌 PLOS ONEに掲載されました。
【用語説明】
注1. 先天性腎性尿崩症(cNDI)
腎臓のV2Rやアクアポリンの変異によって、多飲・多尿などの症状を示す指定難病。本研究では、部分型先天性腎性尿崩症を引き起こすV2R遺伝子(遺伝子シンボルAVPR2)の機能低下型変異(V2Rタンパク質の1アミノ酸残基の置換や欠失)を対象とした。
注2. 2型バソプレシン受容体(V2R)
バソプレシンを特異的に認識するGPCRの1種。腎臓の近位尿細管細胞に発現しており、バソプレシンに結合すると受容体機能がオンとなり、細胞内の三量体Gsタンパク質を介して、アデニル酸シクラーゼの酵素活性を増強させ、cAMP の産生を誘導する。
注3. OPC5アナログ
大塚製薬株式会社によって開発されたV2Rを活性化させるOPC51803(本研究ではOPC5と略称)とその類縁化合物の総称。cNDIの治療薬の候補としてOPC5はラットにおいて抗利尿作用が確認されている。本研究では10種類のOPC5アナログを用いてシグナル伝達の評価を行った。
注4. ドッキングシミュレーション
コンピューターを用いた手法の一つであり、リガンドがターゲットとなるタンパク質の受容体の結合部位にどのように結合するか予測する技術。本研究では構造が明らかとなっているV2RとGタンパク質の複合体構造を用いて、OPC5アナログのドッキングシミュレーションを行った。
注5. バソプレシン
抗利尿ホルモンとも呼ばれるペプチドホルモン。腎臓における水の再吸収を促進させることで、体内の水分や塩分の体外への排出を妨げる。
注6. Gタンパク質共役型受容体(GPCR)
細胞膜表面に存在する受容体タンパク質であり、細胞膜を7回貫通する特徴的な構造を持つ。特定のホルモンなどの細胞外の物質と結合することで細胞内に情報伝達を導く。すなわち、細胞外の情報を細胞内へ伝達する際に最も重要な機能を果たす。
注7. 野生型
健常人で最も多く存在するV2Rのアミノ酸配列を野生型と呼ぶ。先天性腎性尿崩症患者では、V2R遺伝子(遺伝子シンボルAVPR2)に変異が生じることで、V2Rタンパク質のアミノ酸残基に置換や欠失が生じ、野生型V2Rタンパク質とは異なる性質を持つようになる。
【問い合わせ先】
東北大学大学院薬学研究科
教授 井上 飛鳥(いのうえ あすか)
電話 022-795-6860
E-mail iaska@tohoku.ac.jp
.png)